来源:本站 时间:2023.10.13
导读
北京时间2023年10月2日下午,诺贝尔生理学或医学奖宣布授予德国生物技术公司BioNTech的卡塔琳·卡里科(Katalin Karikó)、美国宾夕法尼亚大学教授德鲁·魏斯曼(Drew Weissman),以表彰他们在核苷碱基修饰方面的发现。二者的突破性发现从根本上改变了我们对mRNA与免疫系统相互作用的理解,并使得开发出针对COVID-19的有效mRNA疫苗成为可能,在我们这个时代最大的健康危机之一期间做出了重要贡献。
早在20世纪90年代,卡塔琳·卡里科在宾大担任助理教授时就和时任卡里大学免疫学教授的德鲁·魏斯曼开始了合作,重点研究不同RNA类型如何与免疫系统相互作用。2005年,两人发现当mRNA中包含碱基修饰时,炎症反应可以几乎被消除,这一研究结果对于使用mRNA进行治疗具有深远的意义。在2008年和2010年的进一步研究结果中表明,与未修饰的 mRNA 相比,碱基修饰生成的 mRNA 的递送还显著增加了蛋白质产量。可以说,这些研究成果消除了mRNA在临床应用上的关键障碍,为COVID-19 mRNA疫苗的开发奠定了坚实的基础。
图1. 2023年诺贝尔生理学或医学奖
(图片来源:诺贝尔奖官网)
一、mRNA疫苗发展历程
mRNA从发现到首个产品上市历时约60年时间,许多关键性的研究推动了mRNA在医学上的应用。mRNA发展历程主要分为三个阶段。第一个阶段是mRNA的发现和认识阶段,上个世纪60年代,细胞分子生物学取得了巨大的发展,科学家在对核酸的全面探索中发现了mRNA分子。随后,对mRNA分子的研究主要集中在了解mRNA分子的结构和功能、在真核细胞中的代谢,包括与mRNA重组工程相关工具的开发等领域。进入20世纪70年代,研究人员通过脂质体将mRNA分子传递至细胞中进而诱导蛋白的表达,由此产生了第一个用于mRNA分子传递的阳离子脂质体。第二个阶段是mRNA技术的应用阶段,自20世纪90年代起,经过了三十多年科学的持续进步,mRNA开始在动物体上进行试验。随后一系列里程碑般的实验展露出了基于mRNA治疗的潜力,包括注射流感mRNA诱导小鼠的免疫反应(1993年),注射mRNA疫苗用于小鼠的抗癌研究(1995年),利用改造RNA用于抑制小鼠的丙型肝炎病毒(2002年)等一系列突破性研究,这些研究的方法和成果也完善了基于mRNA治疗在不同领域的发展。进入2000年后,mRNA逐渐开始被应用于传染病疫苗接种、癌症研究等临床前评估中。第三个阶段则是mRNA的高速发展阶段,自2020年开始,伴随针对新冠病毒的mRNA疫苗的正式获批及应用,更是直观地展现出了mRNA技术的巨大潜力,为传统疫苗和药物研究提供了一种全新的替代方案,mRNA自此进入了高速发展的阶段。
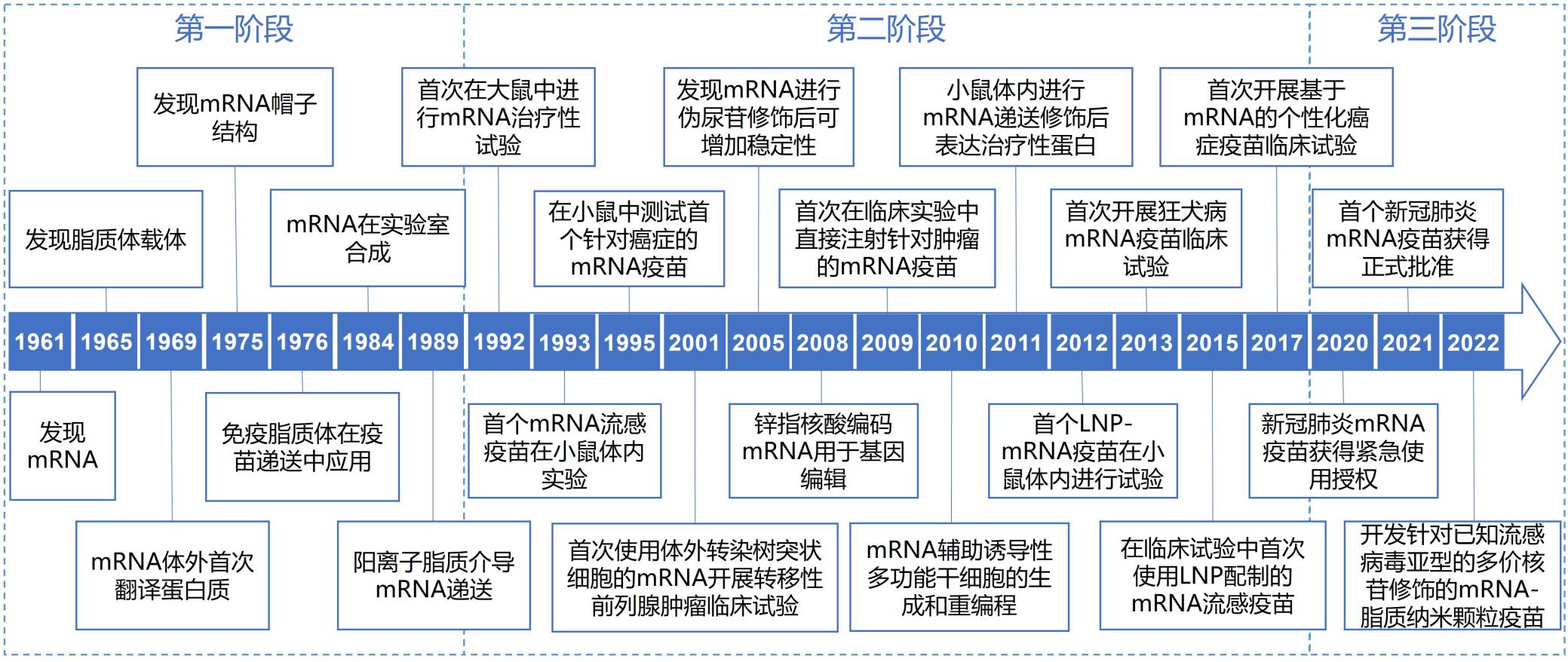
图2.mRNA药物发展历程
(图片来源:《全球mRNA疫苗和治疗药物研究分析报告》)
二、mRNA疫苗技术简介及应用领域
原理
mRNA疫苗技术的基本原理是基于中心法则,在体外合成含有编码特定蛋白的mRNA基因序列,再经过序列优化、化学修饰和纯化等加工,递送至人体细胞,利用宿主细胞翻译产生靶蛋白、刺激宿主产生特异性免疫学反应,进一步使机体获得免疫保护的一种核酸机制。
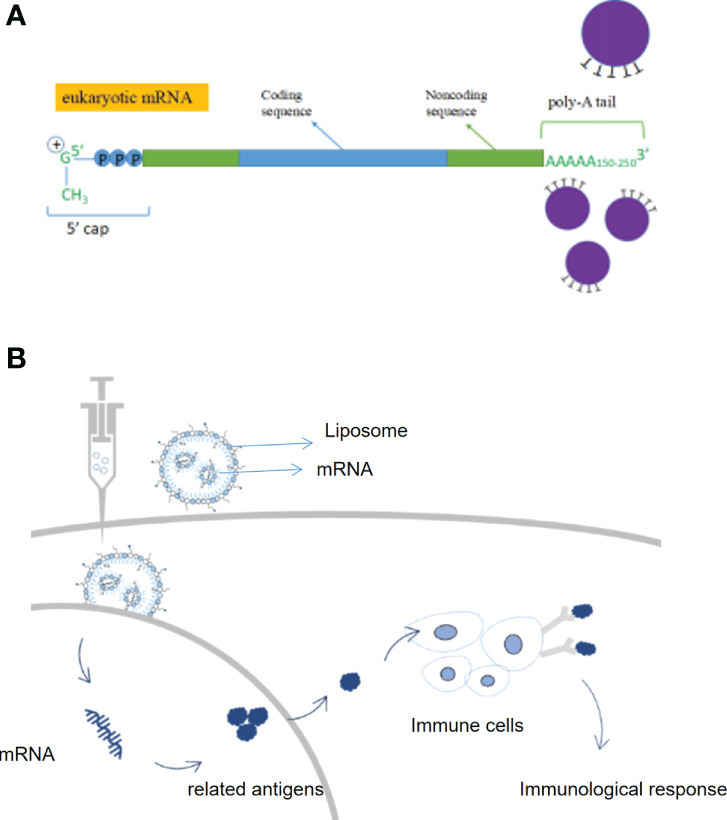
图3. mRNA技术作用原理
(图片来源:Frontiers in Immunology)
优势
与传统疫苗相比较,mRNA疫苗具有如下优势:首先,mRNA具有更强的免疫原性。mRNA除了可以表达特定序列的靶蛋白诱导特异性免疫反应外,作为核酸类的免疫原,还可以诱导人体的天然免疫反应,使其拥有“自我佐剂”(self-adjuvant)的特点;第二,mRNA疫苗安全性方面具有优势。mRNA疫苗的递送不需要特定的质粒载体,不进入细胞核内部,只需要在细胞质内瞬时表达抗原蛋白,不存在整合到人体基因组上的风险;第三,mRNA疫苗具有生产优势。在成本上mRNA疫苗的GMP生产成本是传统疫苗的五到十分之一。另外,由于化学结构相似,生产和纯化与抗原本身无关,同一条mRNA疫苗的生产线很容易被改造成符合EMA或FDA标准的不同抗原疫苗的生产线,因此,在应对突发传染病时,mRNA疫苗很容易在短时间内完成研发和生产。
关键技术
在mRNA疫苗生产中,决定企业行业地位的重点技术环节是:目标靶点的序列选择、mRNA 的设计优化、递送载体封装、生产质控和大规模产业化。决定mRNA疫苗竞争格局的要点与瓶颈集中在两大因素上:mRNA序列结构和疫苗递送系统。
(1)mRNA序列结构
疫苗产生的抗原蛋白的序列以及稳定性决定了其激活的特异免疫的精确性和活性。而抗原蛋白的序列和结构则由mRNA序列影响和控制。因此,mRNA序列决定了疫苗的质量,也是mRNA疫苗厂商的核心竞争力之一。由于mRNA在体内半衰期较短,且外源的mRNA在体内容易引起免疫反应,想要达到蛋白高表达以及降低mRNA免疫原性的目的,就需要对mRNA序列进行修饰优化。目前,主要的mRNA修饰技术包括5’加帽、编码区修饰和非编码区修饰、3’加PolyA尾等。
(2)递送系统
由于mRNA 是一种平均长度为 2000~2500 碱基的单链长多核苷酸,在进入靶细胞发挥转录功能之前,就会被无处不在的细胞外核糖核酸酶迅速降解。且由于mRNA在生理条件下带负电荷,细胞膜的静电排斥作用也会进一步阻碍mRNA向细胞质的扩散。虽然细胞可以通过内吞的方式捕获mRNA,但据推测,裸露的mRNA 的细胞摄取率小于万分之一。mRNA递送是其向临床应用转化的重要壁垒之一。
理想的递送载体应该要保护mRNA 免受核酸酶消化,能被细胞有效摄取,并且能够逃逸内体将mRNA 转运至胞质溶胶内进行翻译。而克服细胞膜障碍以及逃避核酸酶的消化也仅仅是有效递送mRNA 进入靶细胞的初始步骤,最佳的递送载体还需要在体内无明显生物毒性和免疫刺激作用。目前已经研发出多种mRNA递送系统,包括脂质纳米粒、聚合物纳米粒、无机纳米粒以及基于蛋白质的类病毒纳米粒。其中,脂质纳米颗粒(LNP)是当前基于mRNA治疗中研究最为广泛和临床最为成熟的递送系统,如国际上Moderna、BioNTech上市的COVID-19 mRNA疫苗就是采用的脂质纳米递送系统。
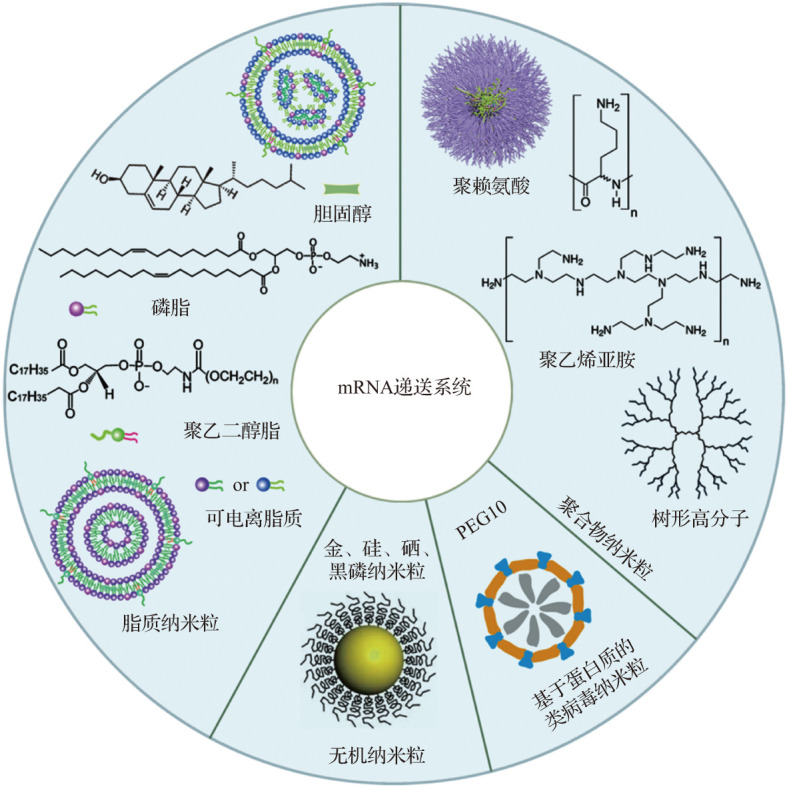
图4. 代表性mRNA递送系统示意图
(图片来源:浙江大学学报)
应用领域
mRNA疫苗技术在难治性疾病或以前无法治愈的疾病,包括传染类疾病、遗传病、癌症、心血管疾病等领域表现出了极大的应用潜力。mRNA新冠疫苗无疑是mRNA技术最大放异彩的应用,但在非新冠的传染病预防方向,流感、人类免疫缺陷综合征、狂犬病和呼吸道合胞病毒感染(RSV)等mRNA疫苗仍值得重点关注。除传染病预防之外,mRNA治疗药物临床研究中,约一半以癌症为主。美国临床试验网站显示,目前全球共有近50项与癌症治疗相关的mRNA疫苗已进入或已完成Ⅱ期临床试验,这些疫苗主要针对黑色素瘤、结肠直肠癌、非小细胞肺癌和头颈部鳞状癌等癌症。另外,mRNA疫苗可在动脉粥样硬化、缺血性心脏病、病毒性心肌炎等心血管疾病领域,通过诱导免疫耐受、调节T淋巴细胞亚群、减轻非特异性炎症反应,使心血管疾病患者获益。
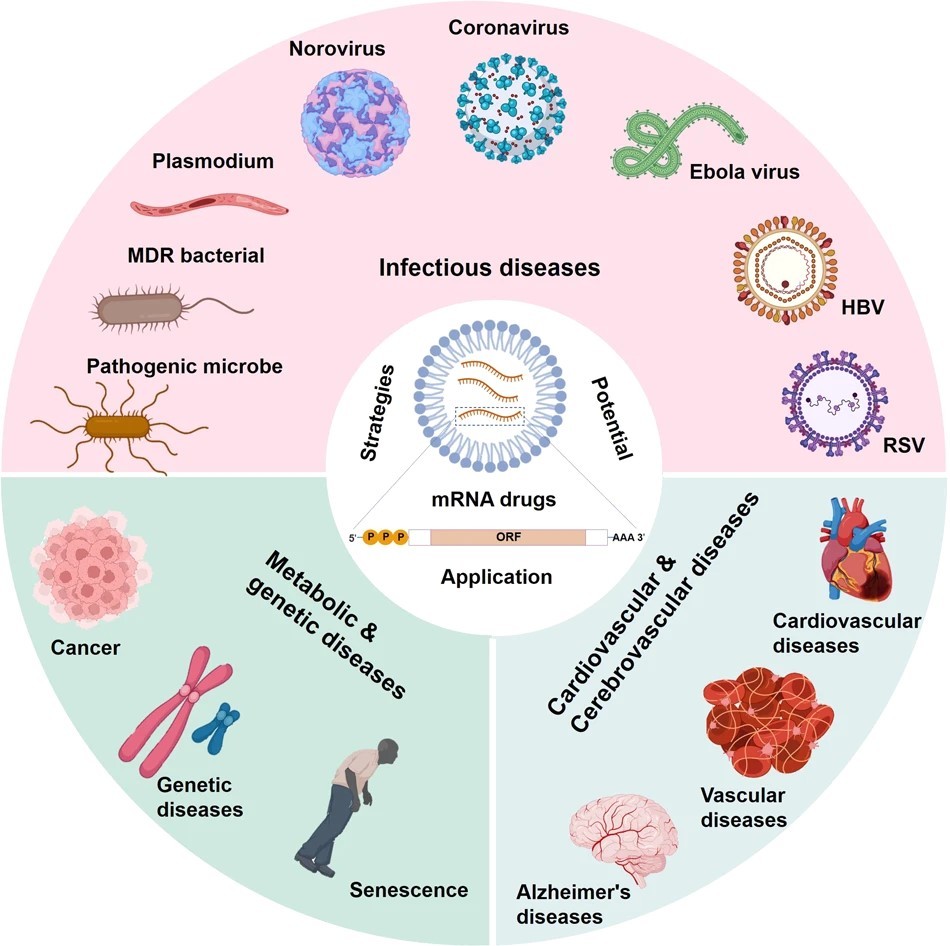
图5. mRNA技术应用领域
(图片来源:Signal Transduction and Targeted Therapy)
三、mRNA疫苗产业简析
根据 2021年发表于Nature Review上的综述分析表明,2021年全球mRNA技术市场主要由新冠疫苗贡献,但市场规模会因新冠病毒的控制、人群的普遍接种而下滑至2025年的约200亿美元;从2025年到2035年,mRNA产品陆续上市,预防性疫苗依然会是支撑市场的基石产品,但随着治疗性疫苗、治疗制剂和mRNA其他新型产品愈发成熟,预计在2035年总市场规模将会维持在230亿美元左右,其中非预防性疫苗可能会占据约110亿美元(48%)。
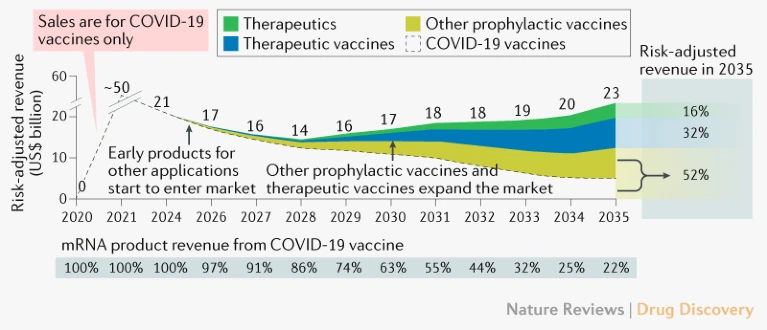
图6. mRNA技术市场演变预测
(图片来源:Nature Reviews Drug Discovery)
从产品及研发管线来看,新冠核酸疫苗是mRNA技术在全球的首个成功应用,也是首次成功大规模商业化。辉瑞、BioNTech以及Moderna凭借新冠mRNA疫苗的布局,获得了亮眼的市场表现。2021年和2022年,跨国制药巨头辉瑞与BioNTech联合开发的mRNA新冠疫苗Comirnaty分别创造营收367.8亿美元和378亿美元,而Moderna生产的mRNA新冠疫苗则分别实现营收177亿美元和184亿美元,Moderna市值更是一度高达2000亿美元。两年间,上述两款明星mRNA产品累计营收超过千亿美元。近几年随着人们对mRNA技术的认知越来越深入,中外药企纷纷开始聚焦该领域的研发。根据ClinicalTrials.gov 相关资料显示,目前全球范围内有超400项处于不同阶段的mRNA疫苗相关的临床研究正在进行中,涵盖了传染性疾病(如流感、RSV、HIV等)和肿瘤(如黑色素瘤、前列腺癌及头颈鳞癌)等适应症。
国内布局mRNA疫苗赛道的企业也较多,除了石药集团的新冠mRNA疫苗在2023年3月被纳入紧急使用开始在国内推广之外,其他管线大多均处于临床前或临床早期阶段。
四、展望
mRNA技术作为2021年全球十大突破性技术之一,更是在2023年获得了诺奖,它随着新冠疫情走上了历史舞台,可以说,其起步于疫苗,但意义要远高于疫苗,是第三波药物浪潮的典范。在未来的几年里,基于科学家们对mRNA疫苗高度的兴趣和市场对其潜力的认可,同时随着mRNA、细胞内载体和体内递送系统的快速发展,我们有理由相信mRNA治疗研究和开发的步伐将不断加快,可能为预防和治疗目前无法治愈的疾病提供新的解决方案。
参考资料:1. How far are the new wave of mRNA drugs from us? mRNA product current perspective and future development. Front Immunol. 2022;13:974433.
2. 全球mRNA疫苗和治疗药物研究分析报告,2023.
3. mRNA-based therapeutics: powerful and versatile tools to combat diseases. Signal Transduct Target Ther. 2022;7(1):166.
4. mRNA药物修饰及其递送系统研究进展. 浙江大学学报. 2023 Aug 25; 52(4):439–450.
5. Evolution of the market for mRNA technology. Nat Rev Drug Discov. 2021,20(10):735-736.





 028-65220888
028-65220888 成都高新区天府大道966号天府国际金融中心南塔28F
成都高新区天府大道966号天府国际金融中心南塔28F